 机制示意图
机制示意图
医学科技创新中心张贵强副教授、宋聪副研究员与附属省立医院魏玉华副主任医师联合团队(医学科技创新中心李松炎博士为文章第一作者)在肿瘤免疫治疗方面取得进展。相关成果以“无载体纳米重塑剂破除肿瘤相关成纤维细胞物理屏障和免疫抑制双重壁垒协同增强免疫治疗(Carrier-free nanoreshapers disrupt cancer-associated fibroblast barriers and alleviate immunosuppression for synergistically potentiated immunotherapy)”为题,于2026年3月17日在线发表于《控制与释放杂志》(Journal of Controlled Release),论文链接:https://doi.org/10.1016/j.jconrel.2026.114835。
在实体恶性肿瘤中,致密的细胞外基质(ECM)和免疫抑制性肿瘤微环境(TME)形成了物理和免疫抑制双重屏障,不仅阻碍了药物的蓄积和渗透,抑制了免疫效应细胞的浸润、活化和功能发挥,最终导致频繁出现耐药性及治疗效果不佳。这一治疗难题在基质丰富的恶性肿瘤(如乳腺癌和胰腺癌)中尤为突出,亟需开发能够同时应对物理屏障和免疫抑制机制的创新策略。
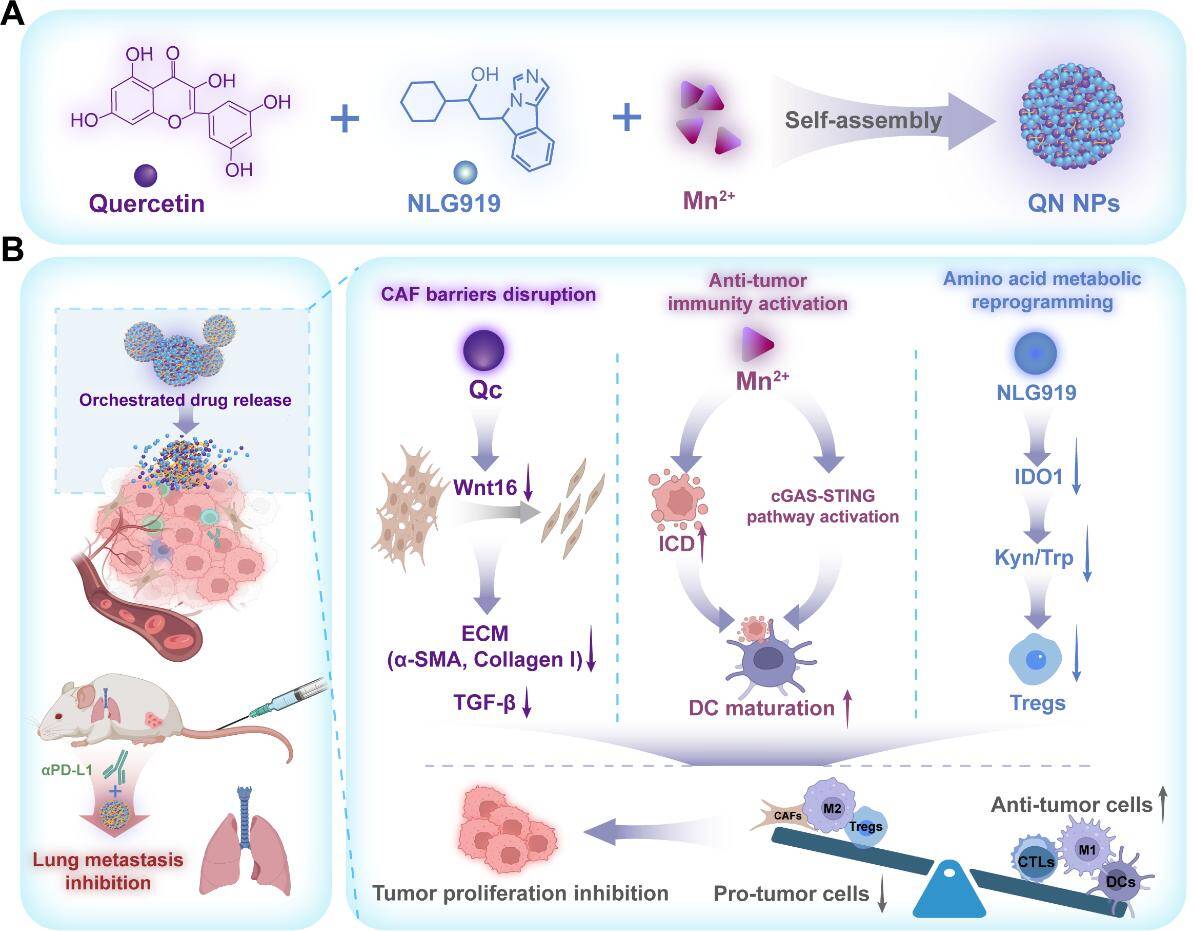
鉴于此,研究团队通过锰离子(Mn2+)与槲皮素(Qc)及吲哚胺2,3-双加氧酶1抑制剂NLG919配位作用,创新性地开发了一种无载体纳米重塑剂(QN NPs)。QN NPs可实现高效的肿瘤富集,并能响应肿瘤微环境触发药物释放。作为活性药物成分,Qc可使癌症相关成纤维细胞恢复正常并减少细胞外基质沉积;Mn2+通过产生羟基自由基诱导免疫原性细胞死亡,并激活干扰素基因刺激因子(STING)通路,从而引发强效免疫应答;NLG919通过阻断犬尿氨酸/色氨酸代谢通路来缓解肿瘤免疫抑制。三者的协同作用共同克服了物理屏障和免疫抑制微环境,从而增强了免疫细胞的浸润和效应功能。此外,将QN纳米颗粒与抗PD-L1抗体联合使用产生了强烈的协同作用,从而显著抑制了原发肿瘤的生长和肺转移。
本研究通过这种化繁为简的设计,将三种功能成分集于一身,药物负载率高达90.1%,规避了传统纳米载体不易降解和载药量低的难题。这种无载体纳米重塑策略克服了间质纤维化和免疫逃逸的双重挑战,为开发基于物理屏障破坏和微环境重编程的联合免疫疗法提供了有前景的范式。
该工作得到了山东省自然科学基金、山东第一医科大学医学科技创新中心大型仪器设备开放共享基金项目的支持。