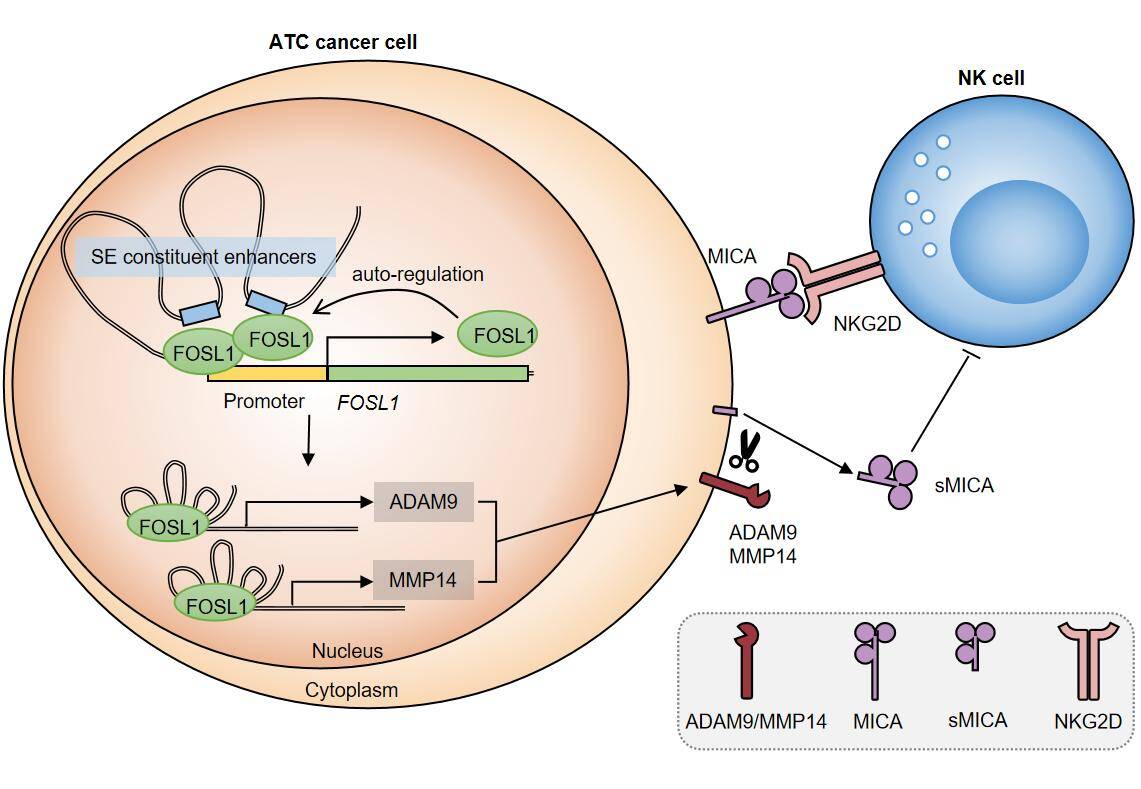
FOSL1介导表观遗传重编程调控ATC免疫逃逸的分子机制模型
生命科学学院杨明教授团队在FOSL1介导表观遗传重编程调控ATC免疫逃逸研究方面取得进展。相关成果以“FOSL1通过调控甲状腺未分化癌的表观遗传重编程进而抑制NK细胞介导的抗肿瘤免疫(FOSL1 Orchestrates Epigenetic Reprogramming of Anaplastic Thyroid Cancer and Suppresses NK Cell-Mediated Antitumor Immunity)”为题,于2026年5月4日发表于《癌症研究》(Cancer Research)杂志,论文链接:https://aacrjournals.org/cancerres/article-abstract/86/9/2184/784010/FOSL1-Orchestrates-Epigenetic-Reprogramming-of?redirectedFrom=fulltext。
甲状腺未分化癌(Anaplastic Thyroid Cancer,ATC)是最具侵袭性的甲状腺癌亚型,患者生存期仅7-10个月。研究通过多组学分析揭示,FOSL1在ATC中通过结合其自身超级增强子形成正反馈调控环路,维持高表达状态。这一表观遗传自调控机制不仅驱动肿瘤细胞增殖、迁移及侵袭,还通过激活ADAM9/MMP14通路促进MICA分子脱落,显著削弱NK细胞识别与杀伤功能,导致肿瘤免疫逃逸。
基于上述发现,团队提出了双重干预策略:一方面靶向抑制FOSL1自调控环路,另一方面联合恢复MICA表达以增强NK细胞疗效。动物实验证实,该策略可有效恢复肿瘤微环境中NK细胞的细胞毒功能,显著抑制ATC肿瘤生长。该研究阐明了FOSL1在ATC恶性转化中的核心作用,揭示了其通过表观遗传重塑与免疫逃逸协同驱动疾病进展的分子网络。
本研究揭示了FOSL1是恶性肿瘤细胞免疫逃逸NK细胞杀伤的关键靶点,研究结果为研发新的ATC免疫治疗策略奠定了基础。
上述研究得到山东第一医科大学新兴战略领域研究培育计划(202404)等项目的支持。
